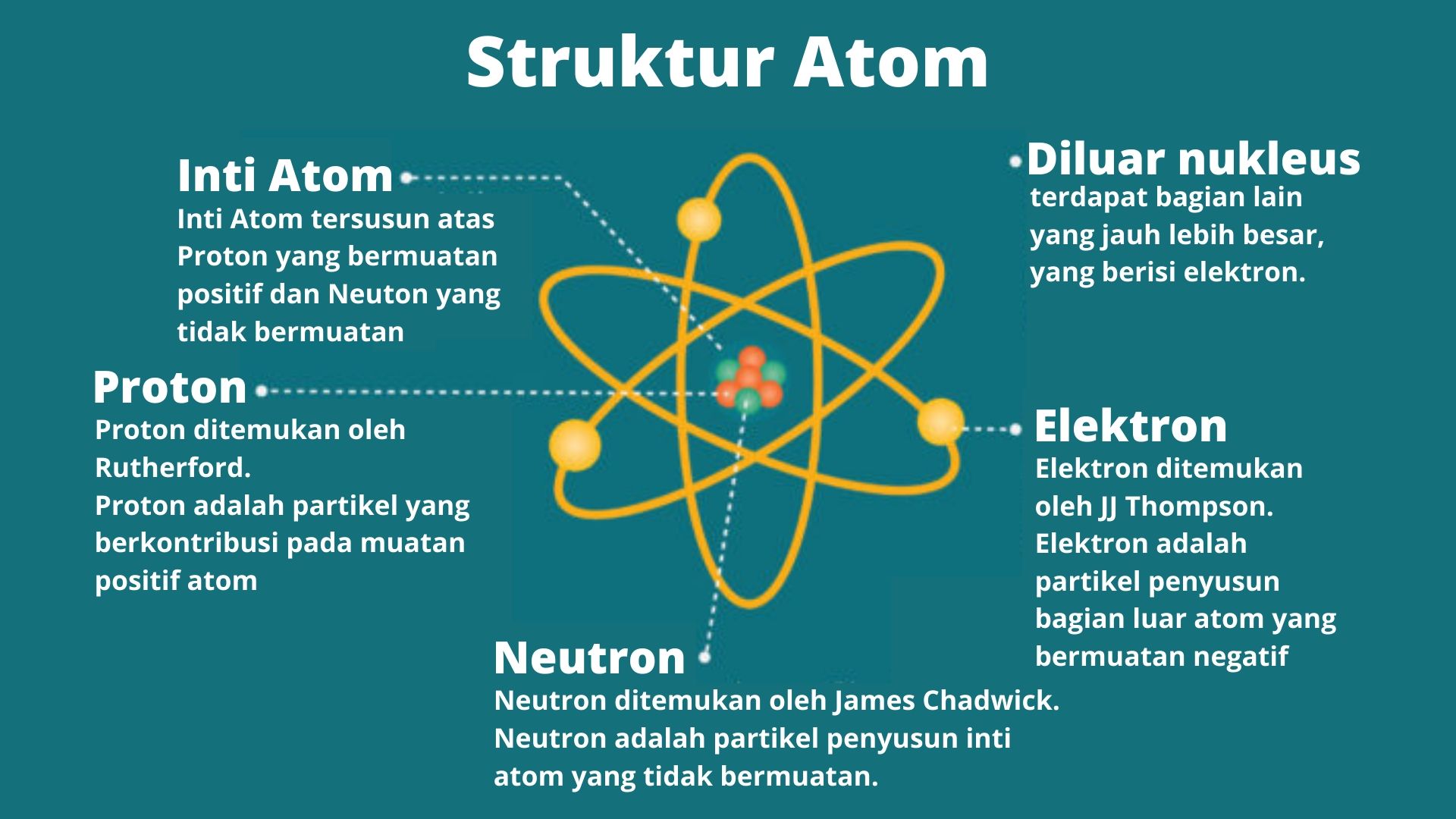
Penjelasan Struktur Atom Proton, Neutron, Elektron dengan Contoh Soal
Konfigurasi elektron adalah penataan elektron ke dalam kulit dan subkulit atom. Sesuai pengertiannya, ada dua cara penulisan konfigurasi elektron, KimiaMath.. karena jumlah elektron yang tersisa adalah 24, sedangkan daya tampung maksimum kulit keempat adalah 32. Perhatikan aturan ketiga yang telah dibahas tadi. Sisa elektron adalah 24.

Berikut Ini Gambar Aliran Elektron Yang Benar Adalah
Selain itu, untuk menentukan unsur tersebut ada pada golongan A atau B adalah jenis subkulitnya. Jika elektron valensinya terletak pada subkulit ns atau ns dan np maka unsur berada pada golongan A, sedangkan jika elektron valensinya terletak pada subkulit ns dan (n-1)d, maka unsur berada pada golongan B. Untuk mengetahui opsi jawaban manakah.
Tuliskan konfigurasi elektronnya dan tentukan pula...
Sehingga dapat ditentukan elektron valensinya, yaitu elektron yang terletak pada kulit terluar suatu atom yang nantinya terlibat dalam pembentukan ikatan kimia. Contohnya: $_{7}N$ : $1s^{2}2s^{2}2p^{3}$, mempunyai elektron valensi 5. Contoh Soal dan Jawabannya. Tentukan konfigurasi elektron untuk unsur-unsur berikut $_{11}A$ $_{15}B$ $_{26}C$
Jelaskan tentang konfigurasi elektron beserta cont...
Dalam teori ini, konfigurasi elektron adalah pengisian elektron yang dimulai dari tingkat energi (kulit) paling rendah, yaitu kulit yang pertama kulit K, setelah kulit K sudah terisi penuh,. Konfigurasi elektron yang berakhiran pada subkulit berlaku aturan penuh setengah penuh. Aturan ini menyatakan bahwa, suatu elektron mempunyai.

Konfigurasi elektron berdasarkan kulit Get Canva
Konfigurasi elektron adalah suatu cara penulisan yang menunjukkan distribusi elektron dalam orbital-orbital pada kulit utama dan subkulit. Pada penulisan konfigurasi elektron perlu mempertimbangkan tiga aturan yaitu prinsip Aufbau, asas larangan Pauli dan kaidah Hund. Prinsip Aufbau Elektron-elektron dalam suatu atom berusaha menempati subkulit-subkulit yang berenergi rendah, kemudian baru ke.

Subkulit Yang Tidak Mungkin Ada Dalam Suatu Atom Adalah Tugas sekolah
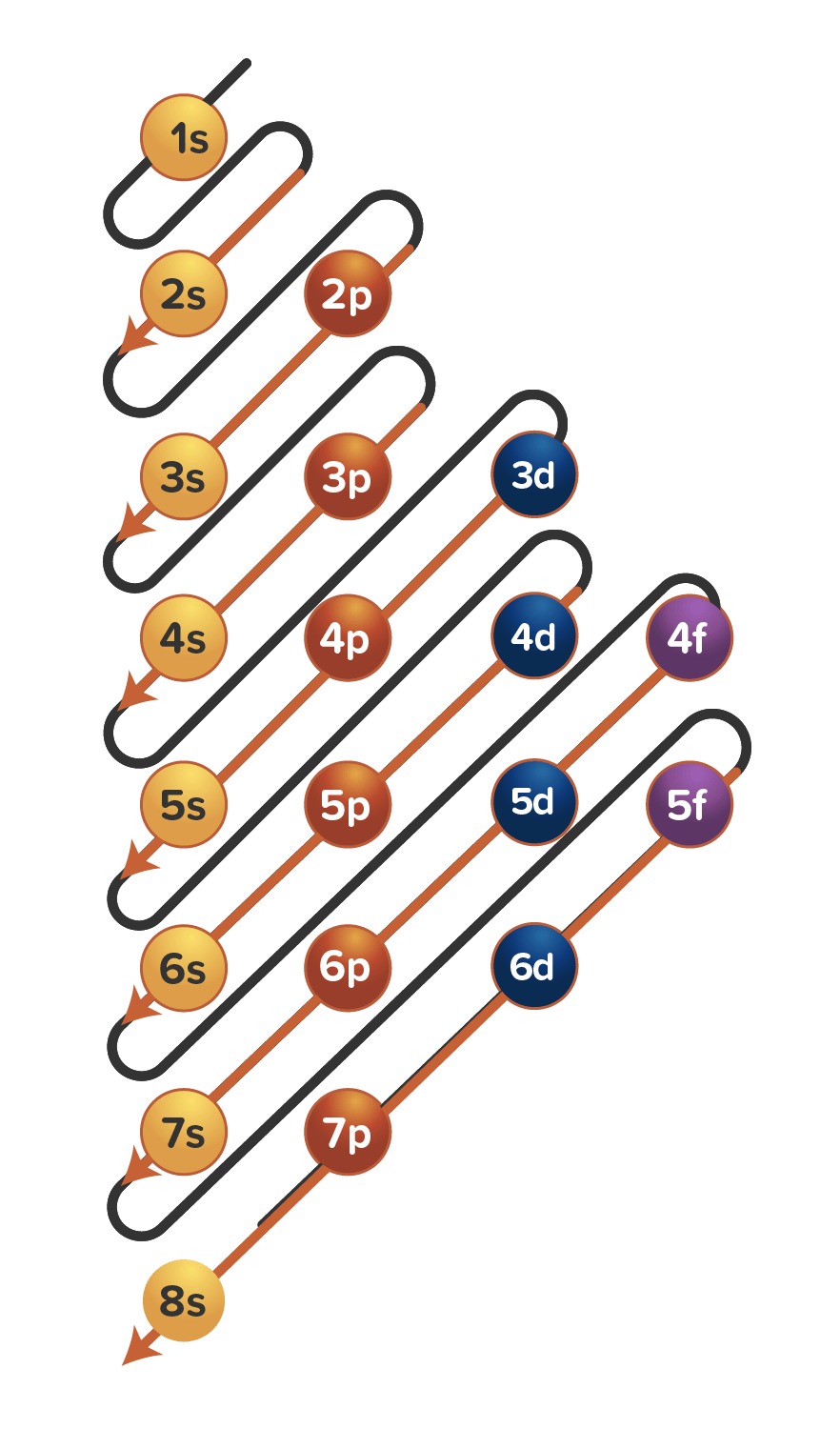
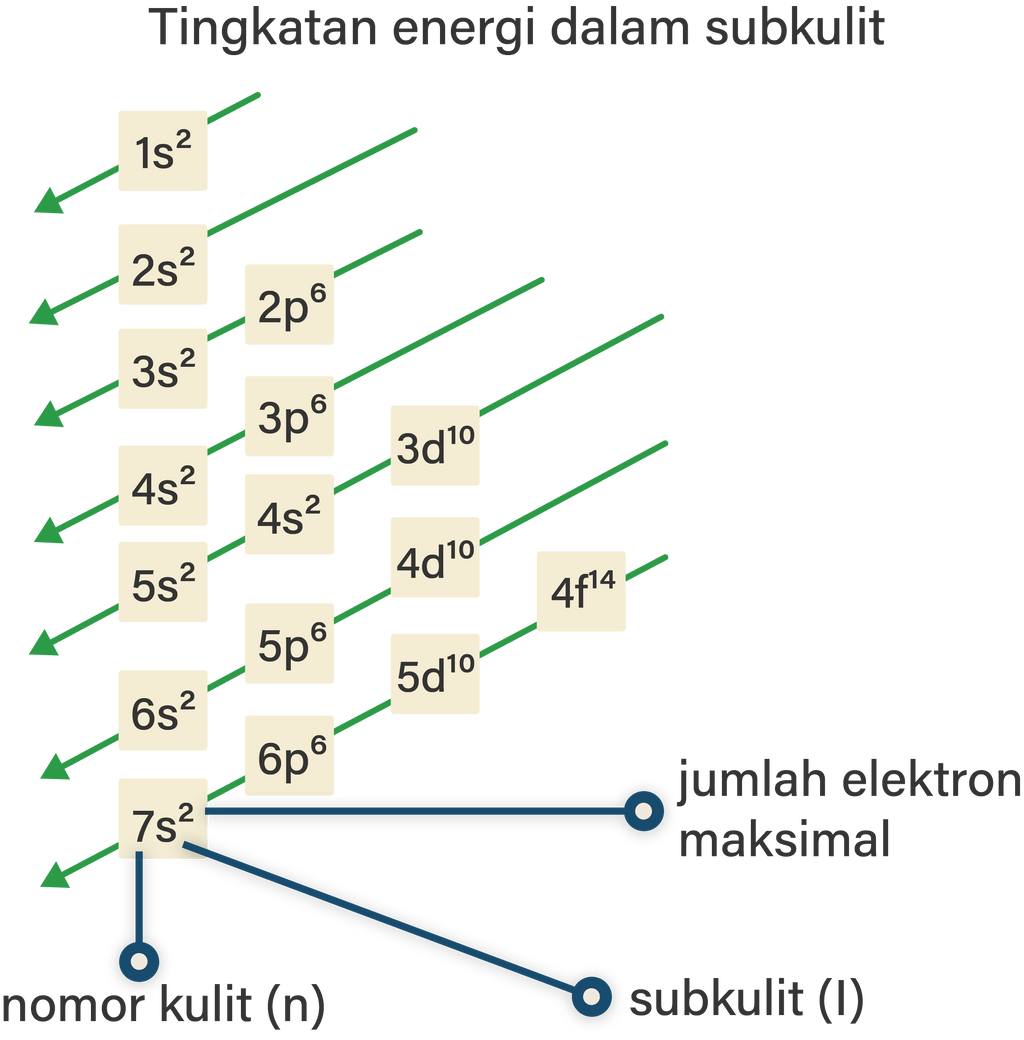
Setelahnya, elektron menempati orbital yang satu tingkat lebih tinggi, dan seterusnya sampai semua elektron dalam atom menempati orbitalnya. Berdasarkan jumlah energi yang dimiliki setiap orbital, urutan pengisian orbital oleh elektron adalah 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6.
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
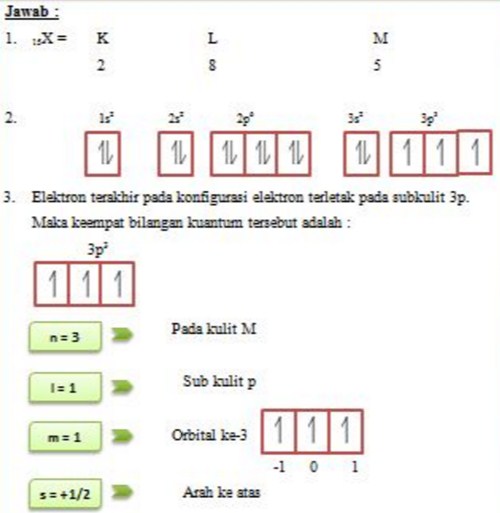
Menuliskan konfigurasi elektron berdasarkan kulit dan subkulit dalam bentuk diagram orbital. 2. Menentukan bilangan kuantum elektron terakhir dari suatu atom.. 2 8 18 18 7 → golongan VIIA Jadi unsur yang terletak pada satu golongan adalah unsur Q dan S yaitu golongan VIA. 12 E (1) Massa atom unsur B lebih kecil daripada unsur C. = artinya.

Konfigurasi elektron suatu unsur adalah 1s^2 2s^2 2p^6 3s...
A. Istilah dalam Konfigurasi Elektron. 1. Kulit Elektron, Subkulit, dan Orbital. a. Kulit Elektron. Kulit elektron adalah lintasan tertentu yang memiliki tingkat energi tertentu yang ditempati oleh elektron-elektron suatu atom. Elektron pada atom menempati lintasan tertentu yang disebut dengan kulit elektron atau tingkat energi.
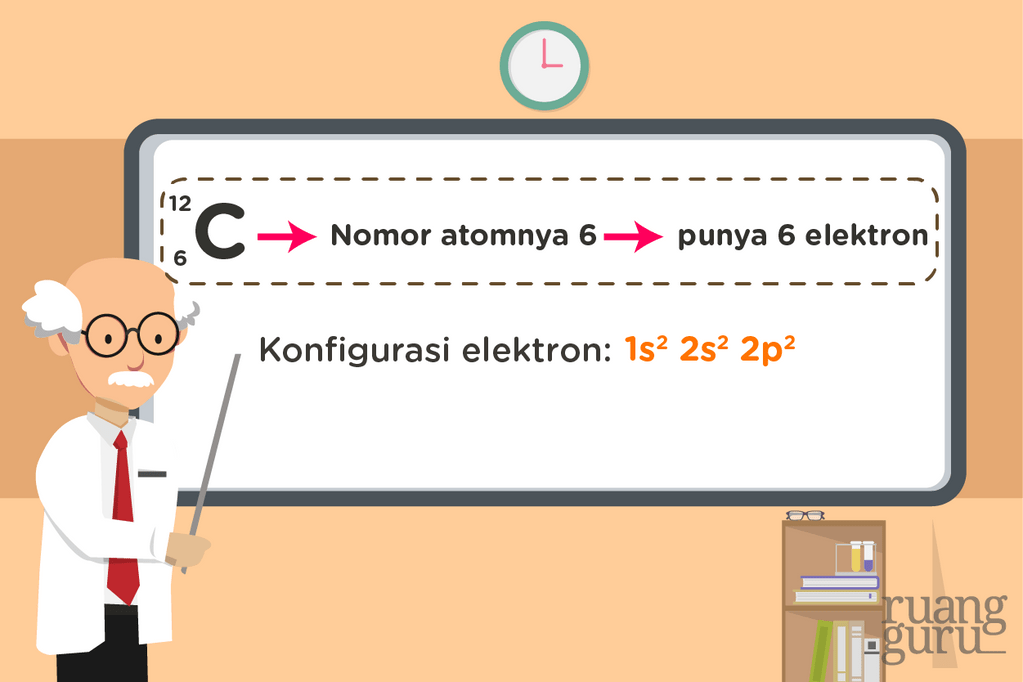
Memahami Konfigurasi Elektron dan Diagram Orbital Lebih Mudah Kimia Kelas 10
Menuliskan konfigurasi elektron berdasarkan kulit dan subkulit dalam bentuk diagram orbital. 2. Menentukan bilangan kuantum elektron terakhir dari suatu atom.. 2 8 18 18 7 → golongan VIIA Jadi unsur yang terletak pada satu golongan adalah unsur Q dan S yaitu golongan VIA. 12 E (1) Massa atom unsur B lebih kecil daripada unsur C. = artinya.

KONFIGURASI ELEKTRON MENURUT TEORI ATOM BOHR & ELEKTRON VALENSI (KIMIA SMA KELAS 10) YouTube
Dalam konteks konfigurasi elektron, "subsidiary" mengacu pada subkulit atau orbital yang diisi dengan elektron. Subkulit subsidi biasanya adalah subkulit dengan energi rendah yang diisi terlebih dahulu sebelum pindah ke subkulit yang lebih tinggi. 4. Apakah ada pengecualian untuk aturan Aufbau? Ya, ada beberapa pengecualian untuk aturan Aufbau.

Bagaimana Kecenderungan Afinitas Elektron Unsur Dalam Sistem Periodik sisi tegak pada bangun
Vanadium termasuk dalam golongan transisi. Elektron valensi dari vanadium tidak terletak di kulit terluar, namun terletak pada kulit ketiga (3d) dan kulit keempat (4s). Jadi, jumlah elektron valensi vanadium adalah 3+2= 5. 4. Seng: (Ar) 3d¹º 4s² Seng termasuk dalam golongan trensisi. Elektron valensi seng hanya terletak pada 4s.
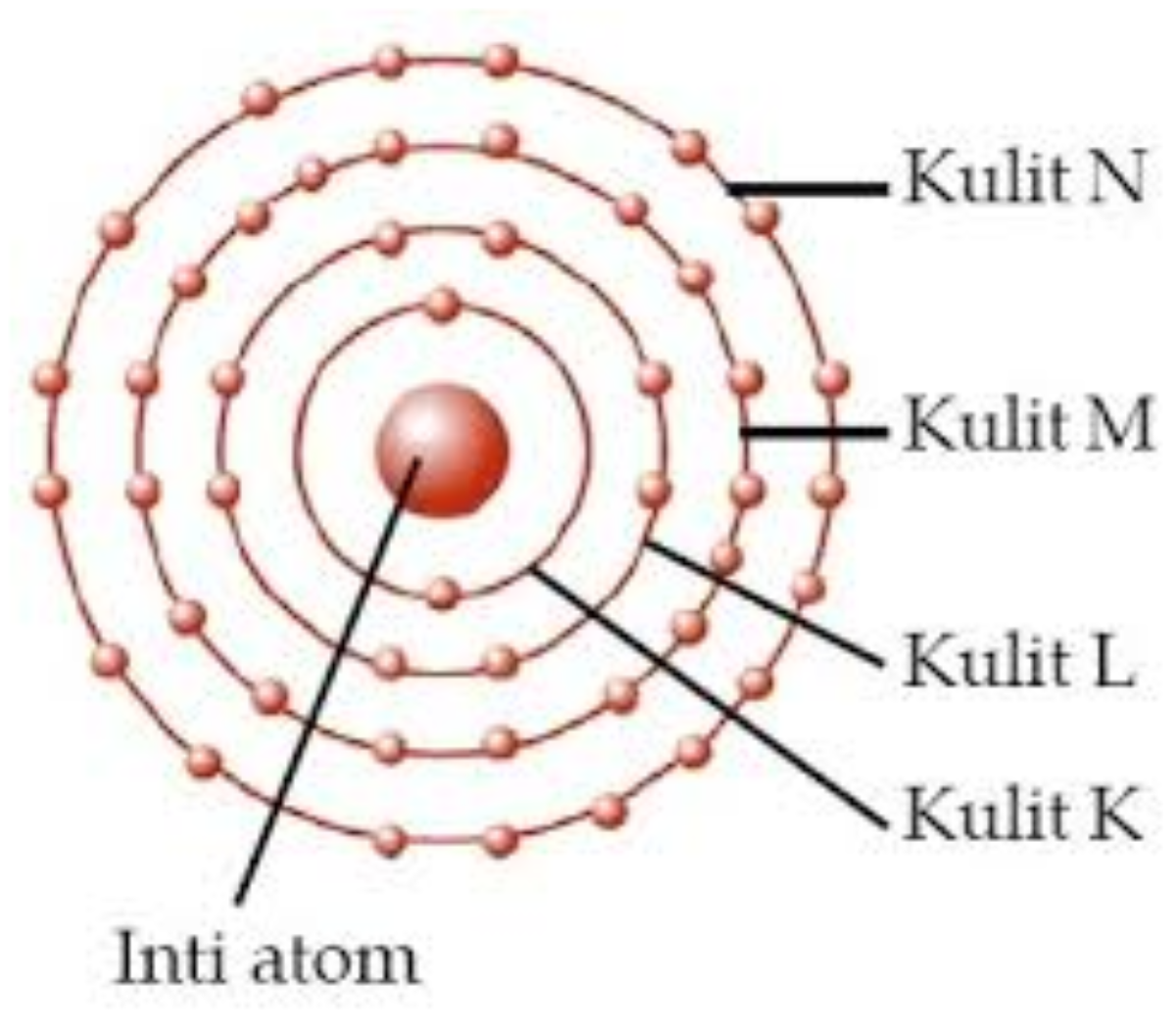
Memahami Kulit Elektron dan Aturan Dasar Penentuan Konfigurasinya Varia Katadata.co.id
Dalam kimia dan fisika atom, kelopak elektron atau kulit elektron dapat dianggap sebagai orbit yang dilalui elektron di sekitar nukleus atom. Kulit yang paling dekat dengan nukleus disebut "kulit 1 " (juga disebut "kulit K"), diikuti oleh "kulit 2 " (atau "kulit L"), kemudian "kulit 3 " (atau "kulit M"), dan seterusnya semakin jauh dari nukleus.

Soal Dan Pembahasan Bilangan Kuantum
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.

Elektron yang terletak dalam satu subkulit adalah YouTube
Pengertian Konfigurasi Elektron. Konfigurasi elektron adalah susunan elektron di dalam atom. Sejatinya, elektron merupakan partikel bermuatan negatif yang berputar mengitari inti atom. Gambaran mudahnya, inti atom dianalogikan sebagai Matahari. Nah, elektron dianalogikan sebagai planet-planet yang berputar mengelilingi Matahari tersebut.

Cara menulis konfigurasi elektron dan mengisi diagram orbital YouTube
Untuk membuat konfigurasi elektron dengan teori mekanika kuantum, ada satu gambar yang harus kalian pahami dulu sebelum membuat konfigurasi elektron berdasarkan orbital atom. Coba perhatikan gambar di bawah ini. Gambar di atas adalah urutan tingkat energi kulit dan subkulit suatu atom. Ada 4 subkulit yaitu s, p, d, dan f.

Pengertian Konfigurasi Elektron Ilmu Kimia
Suatu atom yang mempunyai bilangan kuantum n = 3, ℓ = 1, m = 0, dan s = +1/2, didapatkan. Kulit elektron = 3 (bilangan kuantum n = 3) Subkulit elektron = p (bilangan kuantum ℓ = 1) Karena m = 0, dan s = +1/2 maka diagram orbitalnya. Terdapat 2 elektron pada orbital p, sehingga dapat ditulis . Konfigurasi elektron dari isotop tersebut adalah .