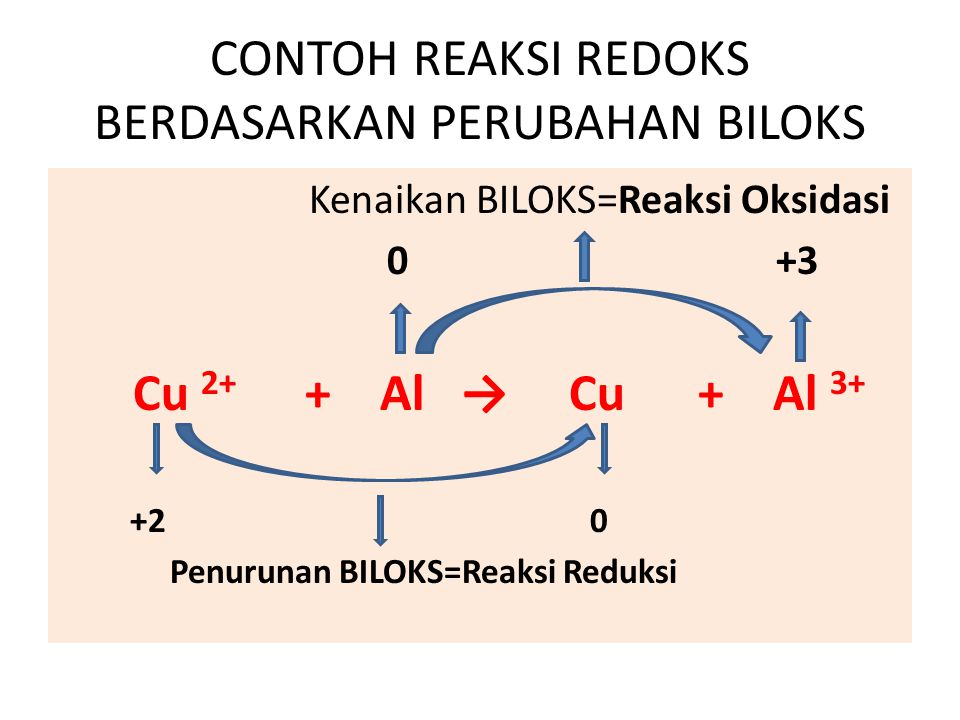
Pengertian redoks berdasarkan perubahan biloks 2021
Kimia Fisik dan Analisis Kelas 10 SMA. Reaksi Reduksi dan Oksidasi serta Tata Nama Senyawa. Bilangan Oksidasi Unsur dalam Senyawa atau Ion. Tentukan biloks Fe pada senyawa kompleks [Fe(CN)6]3-? Bilangan Oksidasi Unsur dalam Senyawa atau Ion. Reaksi Reduksi dan Oksidasi serta Tata Nama Senyawa.

Cara Menentukan Biloks Berdasarkan Prioritas YouTube
Biloks atau bilangan oksidasi suatu unsur adalah bilangan yang menunjukkan sumbangan muatan suatu atom unsur pada molekul atau ion yang dibentuknya. Bilangan oksidasi sering disingkat dengan b.o. Bilangan oksidasi suatu unsur pada suatu senyawa umumnya sama dengan jumlah elektron yang dilepas atau dipasangkan oleh satu atom unsur pada senyawa.

Tata Nama Senyawa Kimia, Tak Kenal Maka Kenalan! Halaman 6
Ingat aturan bilangan oksidasi yang mengandung unsur-unsur senyawa adalah 0. Artinya Fe2O3 = 0. Biloks O = -2. Karena atom O memiliki indeks 3, maka biloks 0 dikaliakan dengan indeks O= -2 x3 = 6. Agar jumlah biloks Fe dan O=0, maka biloks Fe harus bernilai +6. Tapi karena atom Fe punya indeks 2.
Fe Memiliki Biloks Ceritas
Biloks O = -2 Biloks Fe = 6/2 = +3. Jadi, yang merupakan reaksi oksidasi adalah FeO (biloks Fe mengalami kenaikan dari +2 menjadi +3) Dan yang mengalami reaksi reduksi adalah O 2 (biloks O menurun dari 0 menjadi -2). Konsep dan pemahaman reaksi redoks itu sendiri, secara umum memakai konsep kenaikan dan penurunan bilangan oksidasi.

Soal Tentukan biloks Fe pada senyawa kompleks [Fe(CN] 6 ] 3+?
Biloks suatu unsur akan sama seperti muatannya, sehingga untuk menentukan biloks Fe pada senyawa FeCl3 dapat dilakukan dengan menguraikannya terlebih dahulu. FeCl3 → Fe3+ + 3Cl- Dari reaksi di atas dapat kita ketahui bahwa biloks Fe = +3 dan biloks Cl = -1. Semoga bermanfaat ^_^. Beri Rating. · 4.3 ( 3)

PENENTUAN BILANGAN OKSIDASI (BILOKS). YouTube
Dalam kimia, bilangan oksidasi, biloks, atau keadaan oksidasi, adalah muatan hipotesis sebuah atom jika semua ikatannya dengan atom yang berbeda sepenuhnya ionik. Bilangan ini menggambarkan tingkat oksidasi. Dalam kristal Fe 3 O 4 di bawah suhu 120 K (−153 °C), dua pertiga kationnya adalah Fe 3+ dan sepertiganya adalah Fe 2+,.

Kenapa yaa biloks Fe bisa +2 dan +3 🤔🤔 YouTube
Berapa bilok Fe (OH)2. Kimia. Kimia Fisik dan Analisis Kelas 10 SMA. Reaksi Reduksi dan Oksidasi serta Tata Nama Senyawa. Bilangan Oksidasi Unsur dalam Senyawa atau Ion.

Fe Memiliki Biloks Ceritas
Tanpa tahu biloks reaksi redoks dapat disetarakan. Penyetaraan reaksi: Fe(OH)2 + O2 → Fe(OH)3 + OH- (suasana basa) menggunakan metode setengah reaksi tanpa p.

Fe2O3 3Co 2Fe 3Co2 Studyhelp
Oke, kita lanjut ya bahasannya! Pada reaksi redoks, terdapat unsur-unsur yang bertindak sebagai reduktor dan oksidator. Zat yang mengalami oksidasi itu disebut reduktor, sedangkan zat yang mengalami reduksi disebut oksidator. Coba perhatikan contoh berikut ini, ya! Reaksi: Mg(s) + 2HCl ------> MgCl2(aq) + H2(g) Karena Mg merupakan unsur bebas, jadi biloks Mg = 0. Kemudian,

Tentukan biloks dari FeCO3 Brainly.co.id
Agar jumlah biloks Fe dan O = 0, maka biloks Fe haruslah bernilai +6. Tapi, karena atom Fe punya indeks 2, maka biloks Fe : indeks Fe = +6 : 2 = +3. Jadi, biloks Fe 2 = +3. 2. Cr 2 O 7 2-Untuk soal poin b, kita diminta untuk menentukan biloks Cr dalam ion Cr 2 O 7 2-. Ingat aturan biloks nomor 5, jumlah bilangan oksidasi unsur yang membentuk.

biloks Fe kok ada +2 dan +3?? YouTube
Bila H berikatan dengan nonlogam = +1. Biloks O dalam senyawa proksida = -1. Bilangan oksidasi O dalam senyawa non peroksida = -2. Senyawa Fe 3 O 4 dapat terurai menjadi senyawa Fe 2 O 3 dan FeO . Sehingga biloks Fe pada masing-masing senyawa dapat ditentukan.

Aturan Penentuan Bilangan Oksidasi (Biloks) Chemistry Castel
Word Equation. Iron + Sulfuric Acid = Iron (Ii) Sulfate + Dihydrogen. Fe + H2SO4 = FeSO4 + H2 is a Single Displacement (Substitution) reaction where one mole of solid Iron [Fe] and one mole of aqueous Sulfuric Acid [H 2 SO 4] react to form one mole of aqueous Iron (Ii) Sulfate [FeSO 4] and one mole of Dihydrogen [H 2] gas.

Cara Mengerjakan Soal Kimia Biloks Read Master
Enter the formula of a chemical compound to find the oxidation number of each element. A net ionic charge can be specified at the end of the compound between { and }. For example: ZnCl4 {2-} or NH2NH3 {+}. Enter just an element symbol to show the common and uncommon oxidation states of the element. Use uppercase for the first character in the.

PPT REAKSI REDOKS PowerPoint Presentation, free download ID6334934
Tentukan bilangan oksidasi Fe dalam senyawa Fe2SO4 dan FeSO4 ! Bilangan Oksidasi Unsur dalam Senyawa atau Ion. Reaksi Reduksi dan Oksidasi serta Tata Nama Senyawa. Kimia Fisik dan Analisis.

Penyetaraan Reaksi Redoks Metode Biloks Pada Kondisi Basa 1 YouTube
Bilangan oksidasi atom dalam unsur bebas netral sama dengan nol. Contohnya, biloks Fe, Li, Na, O2, dan P4 sama dengan nol. Bilangan oksidasi ion tunggal atau monoatomik sama dengan jumlah muatan ionnya. Misalnya, biloks Cl- adalah -1 dan biloks Au3+ sama dengan +3.
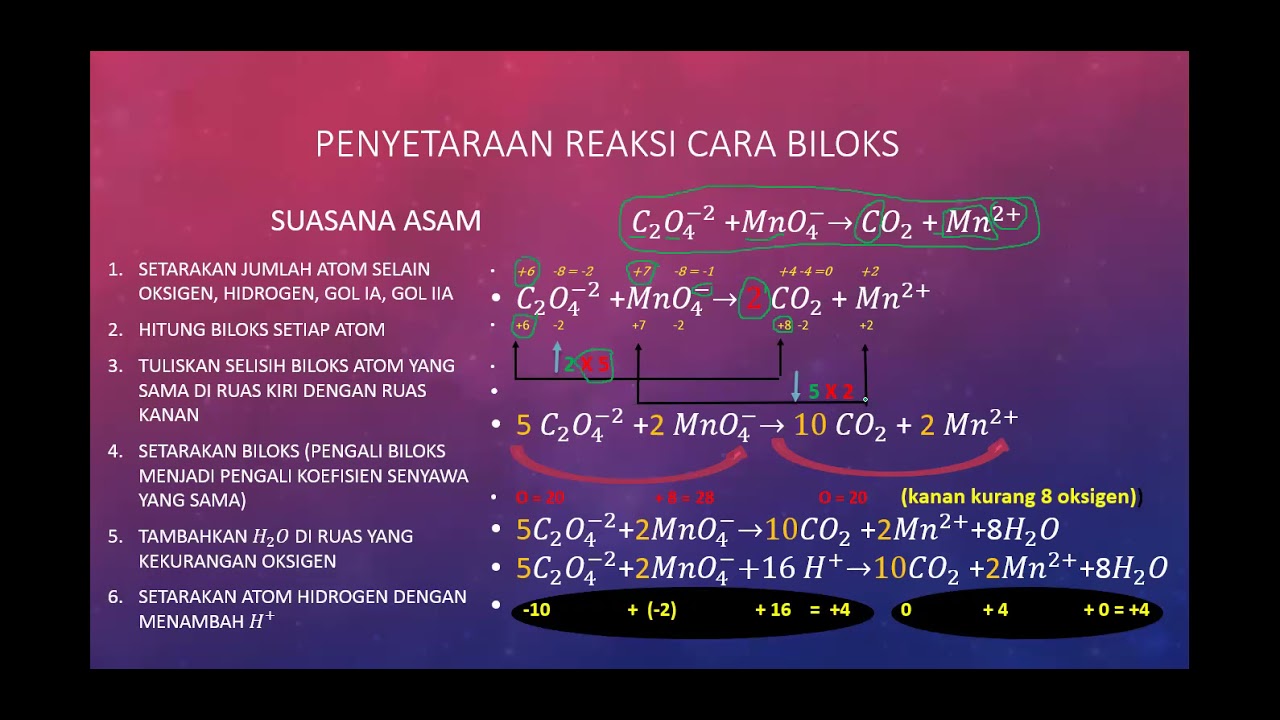
PENYETARAAN REAKSI REDOKS CARA BILOKS YouTube
Bilangan oksidasi ( biloks ) didefinisikan sebagai jumlah muatan negatif dan positif dalam atom, yang secara tidak langsung menandakan jumlah elektron yang telah diterima atau diserahkan. Atom yang menerima elektron akan bertanda negatif, atom yang melepaskan elektron bertanda positif. Dalam bahasa Inggris, bilangan oksidassi adalah oxidation.